近日,本公司收到国家药品监督管理局核准签发的腹膜透析液(乳酸盐-G2.5%)《药品注册证书》(证书编号:2024S00438)及腹膜透析液(乳酸盐-G1.5%)《药品注册证书》(证书编号:2024S00439)。现将相关情况公告如下:
一、药品注册证书的主要内容
1、腹膜透析液(乳酸盐-G2.5%)
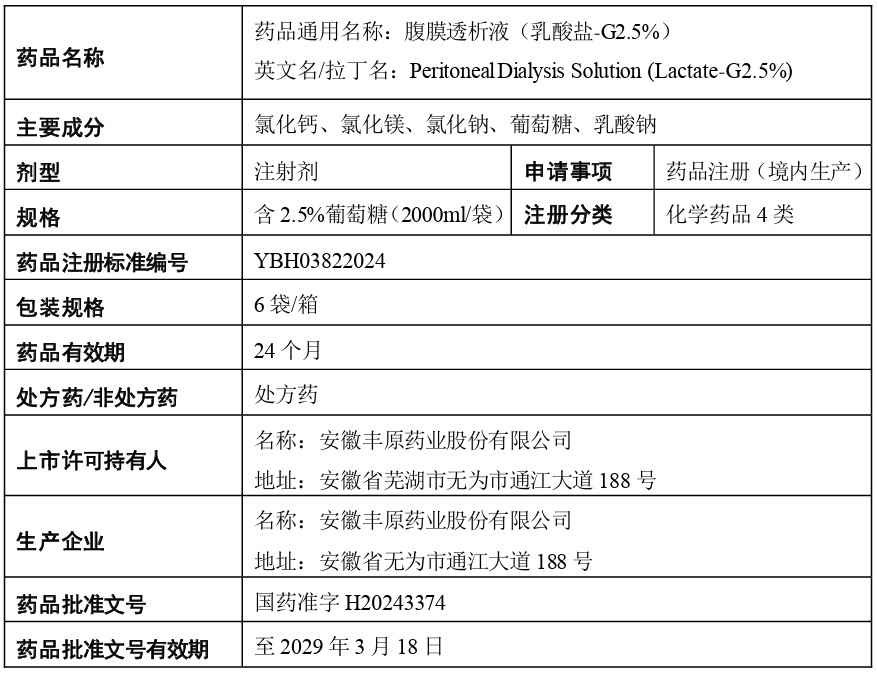
审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准注册,发给药品注册证书。质量标准、说明书、标签及生产工艺照所附执行。药品生产企业应当符合药品生产质量管理规范要求方可生产销售。
2、腹膜透析液(乳酸盐-G1.5%)
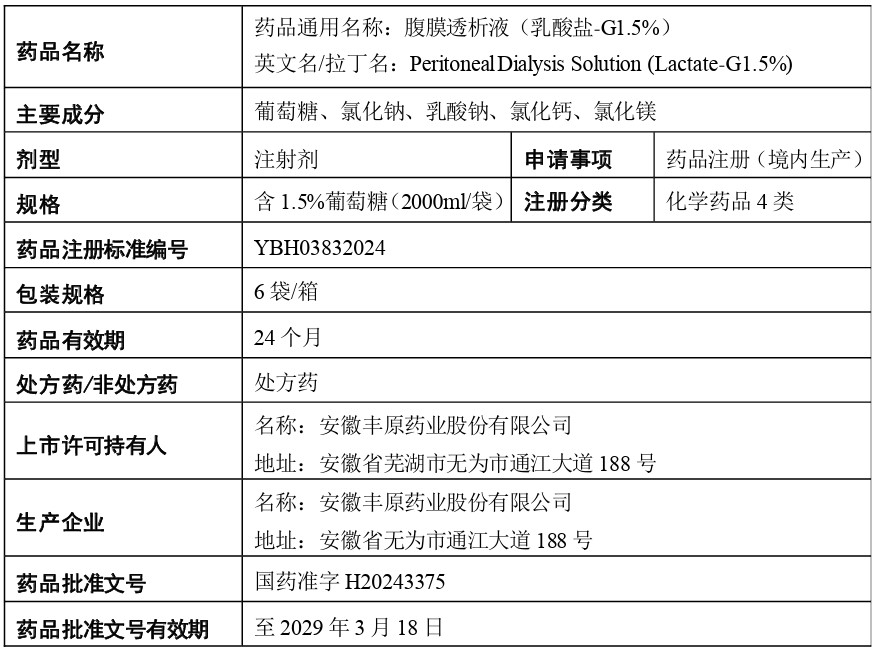
审批结论:根据《中华人民共和国药品管理法》及有关规定,经审查,本品符合药品注册的有关要求,批准注册,发给药品注册证书。质量标准、说明书、标签及生产工艺照所附执行。药品生产企业应当符合药品生产质量管理规范要求方可生产销售。
二、药品其他的相关情况
公司本次获得药品注册证书的腹膜透析液(乳酸盐-G1.5%)和腹膜透析液(乳酸盐-G2.5%), 适用于因非透析治疗无效而需要连续不卧床性腹膜透析治疗的急性及慢性肾功能衰竭患者。
根据国家药品监督管理局《关于仿制药质量和疗效一致性评价工作有关事项的公告》(2017年第100号)相关规定,公司本次获得药品注册证书的腹膜透析液(乳酸盐-G1.5%)和腹膜透析液(乳酸盐-G2.5%),视同通过仿制药质量和疗效一致性评价。
三、对公司的影响
腹膜透析液(乳酸盐-G2.5%)及腹膜透析液(乳酸盐-G1.5%)属公司新建年产1000 万袋腹膜透析液项目拟生产的品规,上述腹膜透析液《药品注册证书》的获得,将丰富公司产品线,优化公司产品结构,有利于提升公司的市场竞争力,对公司未来的发展将产生积极的影响。
四、风险提示
由于药品的生产和销售易受到医药行业政策及市场环境变化等诸多因素影响,具有一定的不确定性,敬请广大投资者注意投资风险。
特此公告
安徽丰原药业股份有限公司
董 事 会
二〇二四年三月二十七日








合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2024 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57